Resumen
Las Enfermedades Neuromusculares (ENM) son un grupo de entidades nosológicas muy heterogéneas caracterizadas por una alteración primaria o secundaria de la célula músculo-esquelética. Las enfermedades del sistema nervioso periférico o neuromusculares se presentan con síntomas variados, como debilidad muscular, dolor, pérdida de la sensibilidad, dificultad para caminar, alteraciones musculo esqueléticas en la vía aérea superior que pueden dificultar la ventilación adecuada, algunas enfermedades pueden afectar también al funcionamiento del sistema respiratorio e incluso del cardíaco, pudiendo el sujeto precisar de respiración asistida y soporte vital. Incluso sin la necesidad de enfrentar un procedimiento quirúrgico planificado, como consecuencia, causan discapacidad física y demandan atención médica especializada.
Introducción
Las Enfermedades Neuromusculares (ENM) son un grupo de entidades nosológicas muy heterogéneas caracterizadas por una alteración primaria o secundaria de la célula músculo-esquelética. Las enfermedades del sistema nervioso periférico o neuromusculares se presentan con síntomas variados, como debilidad muscular, dolor, pérdida de la sensibilidad, dificultad para caminar, alteraciones musculo esqueléticas en la vía aérea superior que pueden dificultar la ventilación adecuada, algunas enfermedades pueden afectar también al funcionamiento del sistema respiratorio.

e incluso del cardíaco, pudiendo el sujeto precisar de respiración asistida y soporte vital. Incluso sin la necesidad de enfrentar un procedimiento quirúrgico planificado, como consecuencia, causan discapacidad física y demandan atención médica especializada. Las Enfermedades Neuromusculares (ENM) son un grupo de entidades nosológicas muy heterogéneas caracterizadas por una alteración primaria o secundaria de la célula músculo-esquelética (1). Dentro de este gran grupo se encuentran enfermedades miopáticas de carácter hereditario, que se producen por defectos en los genes necesarios para la correcta función muscular, y se caracterizan por una debilidad muscular progresiva.
Caso Clínico
A continuación, presentamos el caso clínico de un paciente masculino de 35 años de edad y aproximadamente 50 kg. de peso con diagnóstico de distrofia muscular de Duchenne, programado para cirugía de osteosíntesis de fémur izquierdo, por una caída al intentar dar unos pasos para alcanzar su silla de ruedas, bajo anestesia general.
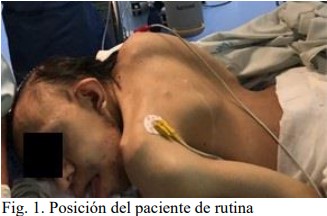 En la valoración preanestésica destacaban graves alteraciones anatómico funcionales del aparato respiratorio por una cifoscoliosis importante, que condicionaba que el paciente no soportara el decúbito dorsal, permaneciendo en todo momento en decúbito ventral (Fig. 1).
En la valoración preanestésica destacaban graves alteraciones anatómico funcionales del aparato respiratorio por una cifoscoliosis importante, que condicionaba que el paciente no soportara el decúbito dorsal, permaneciendo en todo momento en decúbito ventral (Fig. 1).
Varias fracturas patológicas de brazos y
piernas previas provocaban alteraciones
en la conformación de las extremidades,
por lo que hacía difícil también la
posición adecuada en la camilla de
operaciones (Fig.2) 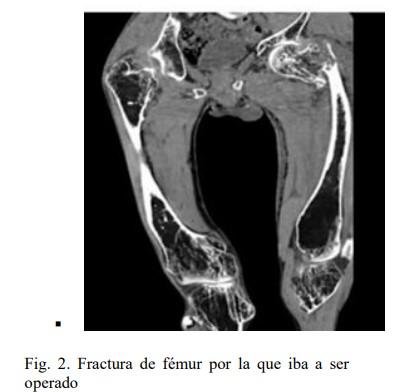
Se consideró que se trataba de una vía aérea difícil conocida por la evaluación los siguientes parámetros:
- Posición inadecuada
- Apertura oral limitada
- Columna cervical deformada y con escasa movilidad
- Cifoscoliosis importante
- Cuello corto Se planificó el abordaje de la vía aérea del paciente y la intubación, con sedación ligera, ventilación espontánea y utilización del fibrobroncoscopio flexible.
No se consideró el manejo de la vía aérea con el paciente despierto porque era un paciente especial que no colaboraba lo suficiente y estaba muy dolorido. El objetivo clave era procurar no perder nunca los reflejos de la vía aérea y mantener siempre al paciente suficientemente oxigenado.
Intubación:
Tras comprobar el buen
funcionamiento de la máquina de
anestesia, se colocó una vía venosa
periférica y se procedió a la
monitorización con oximetría de pulso,
monitor de profundidad anestésica,
monitor de frecuencia cardiaca y
presión arterial no invasiva. Se preparó
el material para el abordaje de la vía
aérea y las drogas respectivas.
El abordaje, de esta vía aérea difícil
conocida, comenzó con una
preoxigenación de más o menos 5
minutos antes de cualquier
administración de drogas. Al alcanzar
una oximetría de pulso superior a 98%,
se inició la administración de
dexmedetomidina a razón de 1ug/kg por
10 minutos, para posteriormente
continuar con una infusión a 0,5
ug/kg/minuto. Se administraron 50mg
intravenosos de lidocaína para
minimizar los reflejos de laríngeos, y
tras 10 minutos, se procedió a la
instrumentación lenta de la vía aérea
con el fibroscopio. Al visualizar la
glotis y observar la movilidad adecuada
de las cuerdas vocales, se instiló
lidocaína según la técnica “spray as you
go”. A continuación, se administraron
40 mg de propofol para conseguir una
sedación momentánea más profunda y
permitir el paso de la fibra y
posteriormente del tubo endotraqueal, lo
cual se consiguió sin ninguna dificultad
y al primer intento, sin cambios
hemodinámicos y sobre todo sin
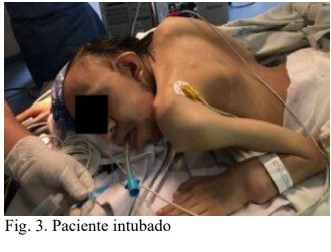
desaturación en ningún momento (Fig.
3).
Con el paciente intubado, se indujo la anestesia general y se indicó al cirujano proceder con la intervención quirúrgica. El procedimiento quirúrgico duró aproximadamente 50 minutos, y al paciente se lo mantuvo con anestesia general balancea, a base de la infusión continua de dexmedetomidina 0,5 ug/kg/min, remifentanilo 0,1 ug/kg/minuto y sevoflorano, sin uso de relajantes neuromusculares y ventilación en modo presión control. No presentó alteraciones hemodinámicas ni de saturación arterial, durante todo el procedimiento.
Extubación: al tratarse de una vía aérea difícil conocida y con los antecedentes del paciente, también planificamos cuidadosamente la extubación, pues sabíamos de antemano que se trataba de una extubación difícil, especialmente porque el paciente no soportaba el decúbito ventral. Treinta minutos antes de la finalización de la cirugía, se administró 1 gr de paracetamol y 5 mg de morfina, para conseguir una analgesia adecuada. Cuando se inició la sutura de la piel, se suspendió la infusión de dexmedetomidina, se instilaron a través del tubo endotraqueal 20 mg de lidocaína para disminuir el reflejo tusígeno y gradualmente se fue retirando el sevoflurano. Se solicitó infiltración de la herida con bupivacaina; al tratarse de una anestesia balanceada, la concentración administrada de sevoflurano fue del 1%, que nos daba una CAM en el monitor de 0,9 al 1. La infiltración al final, en piel, fue realizada con bupivacaina isobara al 0,25%, 14cc en total. Una vez terminada la cirugía y sin agentes anestésicos de por medio, se fue iniciando la recuperación de la ventilación espontanea del paciente, luego de cinco minutos aproximadamente y tras la recuperación total de la consciencia y de la ventilación, se le solicitó al paciente que abriera la boca y con sumo cuidado en inspiración se retiró el tubo endotraqueal, sin ningún problema, ni alteraciones en la ventilación, en la misma posición que se mantuvo siempre (decúbito ventral) y en la misma posición fue trasladado a la unidad de cuidados postoperatorios.
Discusión
El abordaje de la vía aérea es y será siempre un reto para cualquier persona que la maneja, tanto en emergencia como en anestesias planificadas; y para ello tenemos ya conocimiento de factores predictivos que pueden dificultar su abordaje tanto en la ventilación como en la intubación, factores que nos han permitido catalogarlas como vía aérea difícil conocida. Asimismo, este conocimiento de una vía aérea difícil nos ha permitido conocer y capacitarnos en la utilización de diversos métodos para su manejo y para ello disponemos en el mercado de varios dispositivos que mejoran y facilitan su abordaje, tal es el caso de los dispositivos supraglóticos, la videolaringoscopia, la fibra óptica y hasta procedimientos quirúrgicos (2). Este paciente se encontraba en una fase muy evolucionada de su enfermedad. La distrofia muscular de Duchennees una entidad de carácter hereditario recesivo ligado al cromosoma X (las mujeres son portadoras y afecta a los varones), que se presenta en aproximadamente 1 de cada 3500 a 5000 varones nacidos. Está causada por mutaciones en los genes de la distrofina que es una proteína necesaria para la correcta función de las miofibrillas. Sus síntomas se inician a los 3 ó 4 años de vida, y su esperanza de vida, se encuentra entorno a la tercera década de vida, aunque en los últimos años la supervivencia de estos pacientes ha mejorado debido a la intervención temprana en los trastornos respiratorios. En cuanto a los predictores clásicos de vía aérea difícil, el paciente presentaba apertura bucal y distancia tiromentoniana limitadas, así como movilidad cervical reducida debido a los importantes cambios en la estructura de la columna cervical. Además, su saturación basal de oxígeno era de 91% (3). Pero en este caso era especialmente relevante la dificultad que tenía el paciente para soportar el decúbito dorsal, añadiéndose por tanto otro factor de dificultad del manejo de la intubación orotraqueal.
En la enfermedad de Duchenne, las alteraciones musculo-esqueléticas se producen primero en las piernas y pelvis. Más tarde afecta con más severidad a brazos, cuello y otras partes del cuerpo, lo que ocasiona dificultad progresiva para caminar con caídas frecuentes. Las alteraciones musculoesqueleticas también involucran la caja torácica y la columna vertebral, con cifoescoliosis de moderada a grave, que afectan la capacidad respiratoria y muchos pacientes son dependientes de oxígeno. Además, a menudo cursan con trastornos respiratorios relacionados con un defecto restrictivo causado por la debilidad del diafragma, músculos intercostales y accesorios de la respiración, lo que tiene como consecuencia una insuficiencia ventilatoria. Por último, es frecuente el desarrollo de una cardiomiopatía progresiva que involucra la contractilidad tanto del ventrículo izquierdo como del derecho y puede ser génesis de arritmias potencialmente letales (3,4).
Estas alteraciones pueden llegar a causar incapacidad para generar presión espiratoria con tos inefectiva y acumulo de secreciones, que predisponen a episodios recurrentes de neumonía y diferentes grados de insuficiencia ventilatoria que pueden precisar desde asistencia ventilatoria mecánica no invasiva hasta traqueotomía definitiva (5,6,7).
Durante el estudio preoperatorio se valoró la realización de una anestesia regional (raquídea), sin embargo, la severa cifoscoliosis y la dificultad para colocar al paciente en una posición óptima para este tipo de anestesia y el dolor por la fractura, contraindicaba dicha técnica.
Se evitó el empleo de relajantes neuromusculares (RNM). La succinilcolina está directamente contraindicada en estos pacientes por el riesgo de rabdomiólisis, hiperpotasemia y parada cardiaca debido a la inestabilidad de las membranas del sarcolema (8). Por otra parte, los pacientes afectados de la enfermedad de Duchenne presentan un riesgo aumentado de complicaciones pulmonares y cardiacas en el perioperatorio con todos los tipos de sedación o de anestesia, pero este riego es especialmente relevante en el caso de empleo de RNM no despolarizantes. Su uso aumenta las probabilidades de debilidad muscular, recuperación prolongada y complicaciones pulmonares. Deben evitarse en la medida de lo posible, y en caso de ser imprescindibles, administrarse la menor cantidad de agentes de acción corta, y valorar revertir su efecto con el empleo de sugammadex en el caso de haber utilizado relajantes esteroideos.
Tradicionalmente se ha considerado a estos pacientes como de alto riesgo de desarrollo de hipertemia maligna (HM). No sabemos si hay una verdadera asociación genética entre la enfermedad de Duchenne (con alteraciones localizadas en el cromosoma X) y la HM que suele estar relacionada con mutaciones del cromosoma 19. A pesar de lo cual, si parece haber cierta relación entre el empleo de agentes volátiles y el desarrollo de rabdomiólisis e hiperpotasemia severas. El agente que parece estar más relacionado es el halotano en exposiciones prolongadas, pero no se pueden descartar el resto de halogenados. En nuestro caso utilizamos una anestesia general balanceada, basada en la analgesia, con dosis muy baja de sevoflurano y sin relajante neuromuscular, con lo cual nos evitamos cualquier sorpresa en el trasoperatorio. Sin embargo, tal vez podría haberse planteado el empleo de anestesia general intravenosa total (TIVA) (4).
Otro reto, importante en toda vía aérea difícil conocida es el manejo de la extubación ya que no soportaba el decúbito dorsal, por tanto, esta maniobra también debía ser planificada evitando todos los riesgos de complicaciones (laringo y broncoespasmo, dificultad para ventilar, hipoxia, etc.). Para ello tuvimos en mente el algoritmo de extubación de la DAS (Difficult Airway Society). (9)
Paso 1: Planificar la extubación.
Paso 2: Preparar la extubación.
Paso 3: Extubar.
Paso 4: Cuidados post extubación – Recuperación y seguimiento.
En nuestro caso, se trataba de un paciente con una vía aérea difícil fisiológica y una anatomía muy comprometida, con movilidad restringida de la cabeza y el cuello, y alteraciones de columna cervical y torácica. La posición obligada en decúbito prono con acceso restringido a la vía aérea, que ya supuso un desafío en la intubación, podía, si cabe, complicar más el momento de la extubación. Por esto se planificó cuidadosamente la extubación que no se produjo hasta comprobar la recuperación del nivel de conciencia y la ventilación espontánea, resultando exitosa y sin complicaciones.
Por último, se trasladó a la unidad de cuidados postoperatorios, para monitorizar y tratar las eventuales complicaciones postquirúrgicas. Fue dado de alta de este servicio a las dos horas hemodinámicamente estable.
Conclusión
Los pacientes adultos afectados con la enfermedad de Duchenne, suponen un desafío de manejo perioperatorio debido a la escasa reserva cardiorrespiratoria y a las anomalías esqueléticas que pueden asociarse al curso evolutivo de esta patología. Para minimizar los riesgos asociados a cualquier intervención quirúrgica resulta imprescindible planificar de forma cuidadosa todos los procesos implicados.
Bibliografía
1. López-Pisón J, Rebage V, BaldellouVázquez A, Capablo-Liesa JL, Colomer J, Calvo MT et al. Enfermedades neuromusculares hereditarias en pediatría. Nuestra experiencia de 14 años. Rev Neurol 2005;41:145-150. (HTML)
2. Kheterpal S, Han R, Tremper K, Shanks A, Tait AR, O’Reilly M, et al. Incidence and predictors of diffi cult and impossible mask ventilation. Anesthesiology. 2006;105:885-891 (HTML)
3. Domínguez Flores ME, Luna Padrón E, Peñalosa Ochoa L, Galicia Amor S, Toral Freyre S, Baños Mejía BO et al. Guía para el diagnóstico y tratamiento de las alteraciones respiratorias en las enfermedades neuromusculares. Neumol Cir Torax 2011: 70(1): 5-70. (HTML)
4. Gurnaney H, Brown A, Litman RS. Malignant hyperthermia and muscular dystrophies. Anesth Analg. 2009 Oct;109(4):1043-8. doi: 10.1213/ane.0b013e3181aa5cf6. PMID: 19762730. (PubMed)
5. Sunrise medical. Enfermedades neuromusculares ¿Cuál es su origen y sus características? Enero 2020 (HTML)
6. López Vega JM, Calleja J, Combarros O, Polo JM, Berciano J. Motor neuron disease in Cantabria. Acta Neurol Sacand 1988;77:1-5. (PMC)
7. Bach J, Tran J, Durante S. Cost and physician effort analysis of invasive vs. noninvasive respiratory management of Duchenne muscular dystrophy. Am J Phys Med Rehabil 2015; 94(6):474-82 (PubMed)
8. Lerman J. Perioperative management of the paediatric patient with coexisting neuromuscular disease. BJA: Br J Anaesth 2011;107Suppl 1:i79–89. (PubMed)
9. Cooper RM. Extubation and Changing
Endotracheal Tubes. En:Hagberg CA,
eds. Benumof“™s Airway
Management: Principles and Practice.
Philadelphia: Mosby, 2007: 1164-80
(HTML
Correspondencia al autor
Héctor Martínez Villegas
[email protected]
Médico Tratante de Anestesiología
Hospital De Especialidades Eugenio Espejo de
Quito- Ecuador.
Copyright ReAR. Rev Elect Anestesiar pertenece a la Asociación Anestesia Reanimación España. Entidad sin ánimo de lucro.